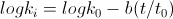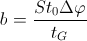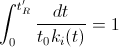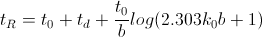Cechą charakterystyczną elucji gradientowej są zmiany siły elucyjnej fazy ruchomej wywołane zmianami składu fazy ruchomej podczas trwania rozdziału chromatograficznego. Gradient modyfikatora organicznego wytwarza się dodając do rozpuszczalnika o mniejszej sile elucyjnej, najczęściej roztworu wodnego, rozpuszczalnika o większej sile elucyjnej, zwykle jest to rozpuszczalnik organiczny (metanol, acetonitryl). Liniowym zmianom siły elucyjnej w czasie t towarzyszą zmiany współczynnika retencji ki:
gdzie:
- k0 – współczynnik retencji odpowiadający składowi fazy na początku gradientu
- b – nachylenie gradientu.
Powyższe równanie można wyprowadzić z równania Snydera-Soczewińskiego, przy założeniu liniowej zmiany zawartości modyfikatora organicznego w eluencie. Nachylenie gradientu b określa szybkość zmniejszania się współczynnika retencji podczas trwania gradientu, kiedy następuje zmiana ułamka objętościowego modyfikatora organicznego Δφ w czasie tG. Czyli:
gdzie:
- S – współczynnik kierunkowy zależności Snydera-Soczewiśnkiego
- to – czas martwy kolumny.
Przebiegi współczynnika retencji, ki¸ dla trzech hipotetycznych analitów w trakcie trwania elucji gradientowej przedstawione są na rysunku:
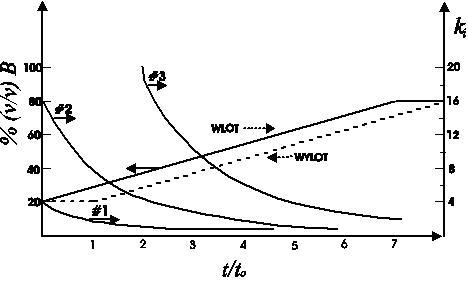
W chromatografii z elucją gradientową podstawowym równaniem opisującym retencję analitu jest zależność:
Znając zmiany chwilowego współczynnika retencji ki w czasie można wyliczyć czas retencji analitu w gradiencie modyfikatora organicznego:
Równanie to jest podstawowym równaniem retencji w przypadku RP HPLC w gradiencie modyfikatora organicznego w eluencie. Zawiera dwie stałe, charakterystyczne dla analitu i dla zastosowanego układu RP HPLC, czyli kolumny oraz eluentu. Są to log k0 i b. Przeprowadzając dwa eksperymenty różniące się czasem trwania gradientu tG w odpowiednio szerokim przedziale gradientu modyfikatora organicznego można, przez rozwiązanie układu dwóch równań, wyliczyć wartości b i log k0. Z kolei, znajomość tych parametrów pozwala obliczyć wartość log kw, czyli standardowy chromatograficzny parametr lipofilowości analitu.
Gradientowo wyznaczone wartości log kw wykazują silną korelację z wartościami wyznaczonymi izokratycznie, zaś procedura gradientowa jest znacznie szybsza. Odpowiednie procedury obliczeniowe znajdują się w handlowo dostępnych oprogramowaniach HPLC (np. DryLab, LC Resources, Walnut Creek, CA, USA; ACD, Advanced Chemical Development, Toronto, Kanada). Znajomość wartości log kw i b pozwala przewidywać retencję analitu w różnych warunkach gradientu modyfikatora organicznego, a także w dowolnych warunkach izokratycznych. Ma to duże znaczenie praktyczne w badaniach nieznanej próbki, gdyż pozwala na jej stosunkowo szybką analityczną charakterystykę oraz na ustalenie optymalnych warunków rozdzieleń składników.
Przykładowe chromatogramy uzyskane w gradiencie modyfikatora organicznego dla 10 analitów przedstawia Rysunek 2:
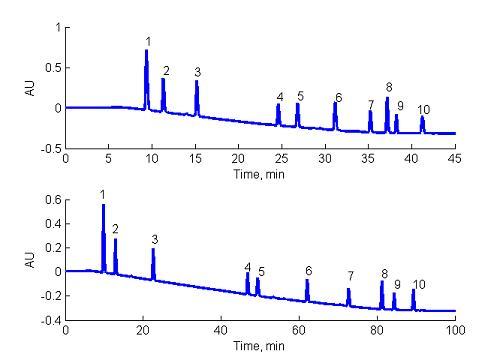
Warunki: aparat – Merck Hitachi LaChrome, gradient metanol-bufor uniwersalny o pH=10.5 (5-80%), kolumna XBridge C18, 150×4.6 mm, 5 μm; temperatura = 25 oC; czas trwania gradietnu 32 i 88 min.
Literatura
- P. Wiczling, R. Kaliszan: Gradientowa RP HPLC , w: Nowoczesne techniki analityczne, pod red. M. Jarosza, Warszawa : Oficyna Wydawnicza Politechniki Warszawskiej, 2006, s. 67-84.
- Snyder L.R., Dolan J.W., Gant J.R., J. Chromatogr. 165 (1979) 3.
- Snyder L.R., Kirkland J.J., Glajch J.L., Practical HPLC Method Development, John Wiley & Sons, Inc., New York 1997