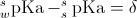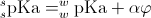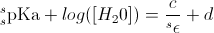Podobna notacja jak użyta w przypadku pH ma też zastosowanie do przedstawiania pKa. Dla przykładu, wartość pKa w rozpuszczalniku s powinna być podana jako sspKa , jeżeli aktywność jonów wodorowych była mierzona w skali sspH lub jako wspKa, jeżeli była mierzona w skali wspH . Analogicznie jak w przypadku pH, obie wartości pKa są powiązane zależnością:
Dodatek modyfikatora organicznego do roztworu zawierającego substancję o charakterze kwasowym bądź zasadowym powoduje zmianę wartości pKa tej substancji. Przykład zmian wartości sspKa w zależności od składu fazy ruchomej, podany przez Rosésa i Bosch, przedstawiony jest na Rysunku 1:
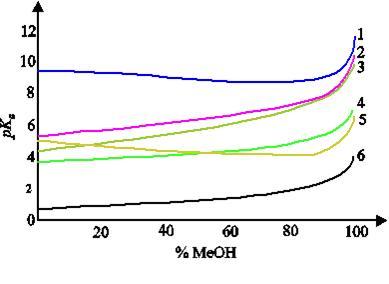
Zmiana wartości pKa ze składem rozpuszczalnika jest charakterystyczna dla każdej substancji. Wynika to z różnej solwatacji substancji przez składniki rozpuszczalnika. Pomimo tej różnorodności, można wyróżnić kilka trendów. Obserwuje się, że kwasów obojętnych (np. kwas octowy) i anionowych (np. diwodorocytrynian) zawsze wzrasta ze wzrostem zawartości rozpuszczalnika organicznego w mieszaninie. Z kolei, pKa zasad obojętnych (np. anilina) i protonowanych (np. amoniak) najpierw obniża się z dodatkiem rozpuszczalnika, a przy dużej jego zawartości gwałtownie wzrasta. Minimum obserwuje się przy zawartości metanolu 90% (v/v).
Wyprowadzono kilka równań, niestety dość skomplikowanych, które opisują zależności między składem fazy a wartością pKa. Dla ograniczonej zawartości metanolu w mieszaninie można jednak przyjąć zależność prostoliniową:
Jednak najczęściej stosuje się równanie Yasuda-Shedlovsky’ego:
gdzie sε oznacza stałą dielektryczną mieszaniny s, zaś c oraz d oznaczają stałe; [H2O] oznacza stężenie wody. Wartość uzyskuje się poprzez serię pomiarów w rozpuszczalniku o różnej zawartości modyfikatora organicznego (różne wartości sε), wyliczenie odpowiadających wartości z równania i ekstrapolację uzyskanych danych do czystej wody, której odpowiada wartość sε = 76,75 oraz wartości log [H2O] = 1,74.
Literatura
- Rosés M., Bosch E., J. Chromatogr. A 982 (2002) 1
- Bosch E., Bou P., Allemann H., Rosés M., Anal. Chem. 68 (1996) 3651
- Rived F., Canals I., Bosch E., Rosés M., Anal. Chim. Acta 439 (2001) 315
- Yasuda M., Bull. Chem. Soc. Jpn. 32 (1995) 429.
- Shedlovsky T., w: B. Pesce (red.), Electrolytes, Pergamon Press, New York, 1962.